Yuanfeng POV: calendrier actualisé de l'EUDAMED
La Commission européenne a récemment annoncé des mises à jour pour la réalisation et la mise en œuvre de l'EUDAMED sur la base de l'amendement 2024/1860.Cet article décrit les délais actuels de l'EUDAMED et notre point de vue sur ces délais afin d'aider l'industrie à se préparer en conséquence.
Échéanciers actuels de l'EUDAMED:
- La date limite pour la première application obligatoire des modules fonctionnels EUDAMED est toujours le 1er janvier 2026.Le module de vigilance devrait être obligatoire à partir du troisième trimestre 2026 et la pleine fonctionnalité d'EUDAMED prévue pour le deuxième trimestre 2027.
- Les modules Actor, UDI & Devices, Certificates et Surveillance du marché sont actuellement à l'étude.L'audit indépendant du produit minimum viable (MVP) vise à évaluer et à confirmer la fonctionnalité et l'interconnectivité des modules jugés prêts pour l'audit.Cet audit devrait être achevé au deuxième trimestre 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Les modules Actor, UDI & Devices, Certificates et Market Surveillance devraient être déclarés pleinement opérationnels à la fin du deuxième trimestre 2025, ce qui conduira à leur date d'application obligatoire du 1er janvier. 2026.
Je suis désolée. - Les modules Actor, UDI & Devices, Certificates et Market Surveillance devraient être déclarés pleinement opérationnels d'ici la fin du deuxième trimestre 2025 et obligatoires pour une utilisation dans l'industrie le 1er janvier 2026.
- Le module de vigilance ne fait pas partie de l'audit en cours sur le MVP et ne sera pas déclaré pleinement fonctionnel avec les modules mentionnés précédemment.Le calendrier révisé indique que l'audit de ce module aura lieu entre le deuxième et le troisième trimestre de 2025, avec pour objectif la date d'application obligatoire au deuxième trimestre de 2026.
Je suis désolée. - Le développement du module d'investigation clinique/études de performance (CI/PS) devrait se poursuivre jusqu'au troisième trimestre 2026.Une vérification visant à évaluer le module CI/PS ainsi que les cinq autres modules (5) sera achevée une fois que le MVP CI/PS aura été élaboré..
Je suis désolée.
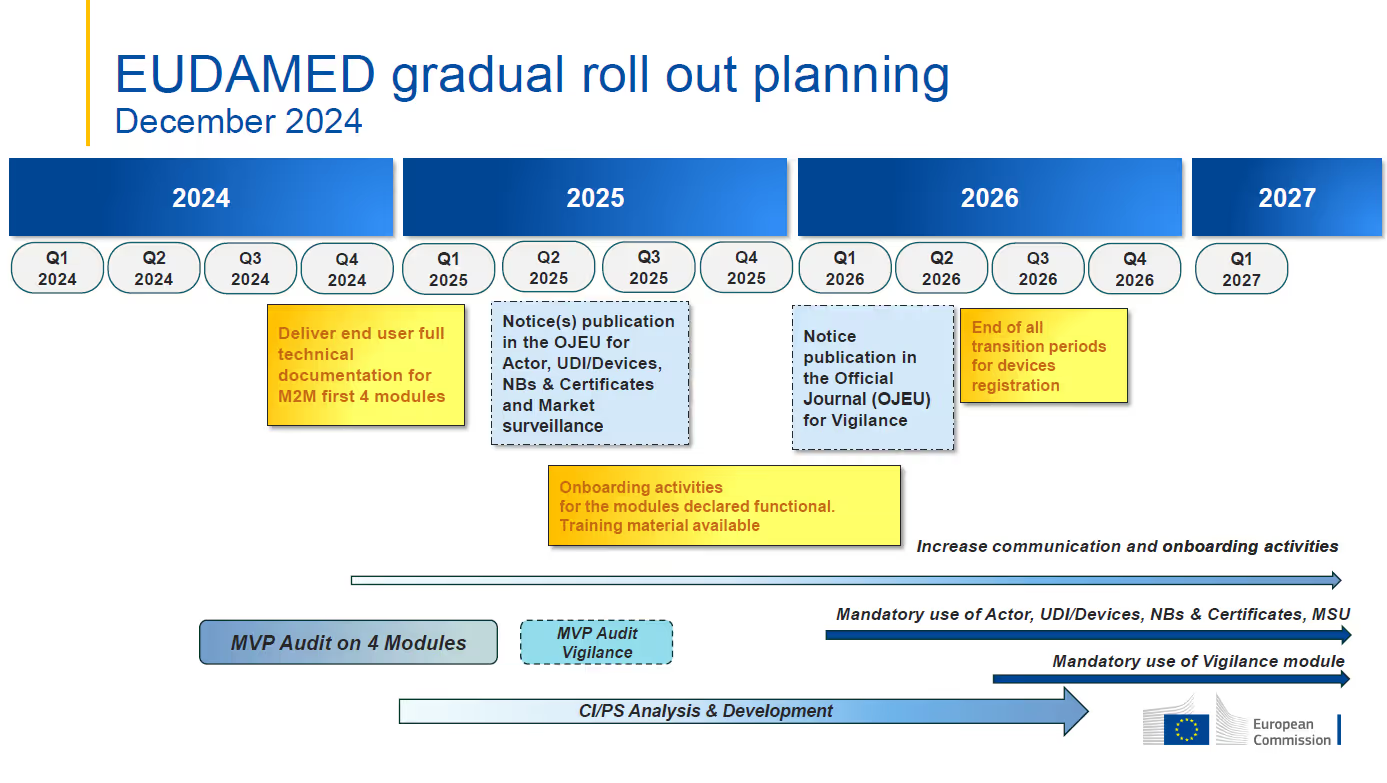
Photo courtesy du groupeLe Parlement européen
La Commission européenne a récemment annoncé des mises à jour pour la réalisation et la mise en œuvre de l'EUDAMED basées sur:modification 2024/1860.Cet article décrit les calendriers actuels de l'EUDAMED et notre point de vue sur ces calendriers afin d'aider l'industrie à se préparer en conséquence.
Échéanciers actuels de l'EUDAMED:
- La date limite pour la première application obligatoire des modules fonctionnels EUDAMED est toujours le 1er janvier 2026.Le module de vigilance devrait être obligatoire à partir du troisième trimestre 2026 et la pleine fonctionnalité d'EUDAMED prévue pour le deuxième trimestre 2027.
- Les modules Actor, UDI & Devices, Certificates et Surveillance du marché sont actuellement à l'étude.L'audit indépendant du produit minimum viable (MVP) vise à évaluer et à confirmer la fonctionnalité et l'interconnectivité des modules jugés prêts pour l'audit.Cet audit devrait être achevé au deuxième trimestre 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Les modules Actor, UDI & Devices, Certificates et Market Surveillance devraient être déclarés pleinement opérationnels à la fin du deuxième trimestre 2025, ce qui conduira à leur date d'application obligatoire du 1er janvier. 2026.
Je suis désolée. - Les modules Actor, UDI & Devices, Certificates et Market Surveillance devraient être déclarés pleinement opérationnels d'ici la fin du deuxième trimestre 2025 et obligatoires pour une utilisation dans l'industrie le 1er janvier 2026.
- Le module de vigilance ne fait pas partie de l'audit en cours sur le MVP et ne sera pas déclaré pleinement fonctionnel avec les modules mentionnés précédemment.Le calendrier révisé indique que l'audit de ce module aura lieu entre le deuxième et le troisième trimestre de 2025, avec pour objectif la date d'application obligatoire au deuxième trimestre de 2026.
Je suis désolée. - Le développement du module d'investigation clinique/études de performance (CI/PS) devrait se poursuivre jusqu'au troisième trimestre 2026.Une vérification visant à évaluer le module CI/PS ainsi que les cinq autres modules (5) sera achevée une fois que le MVP CI/PS aura été élaboré..
Je suis désolée.

Photo courtesy du groupeLe Parlement européen
Voici comment Rimsys considère l'impact de cette annonce pour chaque groupe de parties prenantes:
Le Yuanfeng
L'UDI est à l'avant-plan ainsi que l'interaction future avec le module de vigilance.Comme Rimsys continuera à développer la fonctionnalité UDI et la fonctionnalité de surveillance postérieure du marché indépendamment des dates cibles mises à jourNous reconnaissons également l'impact potentiel de l'établissement de capacités de transfert de données (DTX) pour interagir avec EUDAMED dans une capacité machine-à-machine (M2M).Avec la publication des exigences finales nécessaires pour le M2M DTX à EUDAMED, Rimsys est en mesure de finaliser notre connexion et de fournir des capacités M2M dans le cadre de la solution EUDAMED.
Industrie/client
Comme la Commission européenne a mis à jour à plusieurs reprises les délais de l'EUDAMED, nous nous attendons à ce que l'industrie ait une certaine réticence à accepter les nouvelles dates cibles.Cela pourrait retarder la reprise des préparatifs de l'EUDAMEDCependant, nous ne nous attendons pas à ce que la CE repousse ces délais actualisés.Les fabricants qui n'ont pas prévu de soumettre des données à EUDAMED d'ici au deuxième trimestre de cette année devraient s'attendre à des défis importants pour respecter ces délais.Avec l'audit des modules attendus en cours et la documentation technique associée publiée,Rimsys recommande de prendre des mesures pour organiser les données réglementaires dès maintenant et soumettre leurs informations rapidement à tous les modules EUDAMED disponibles.
Commission de l'UE
La CE recommande fortement à l'industrie de continuer à mettre en place sa solution et de soumettre des données sur une base volontaire.La position de la Commission est que la présentation précoce des données donnera aux entreprises un avantage en leur permettant d'avoir leurs données à portée de main avant l'assaut de l'ensemble de l'industrie mondiale des technologies médicales.Ces entreprises seront également en première ligne pour travailler avec les ressources de la Commission si des problèmes de soumission de données surviennent.
* Remarque - cet article comprend des interprétations réglementaires et des avis duLe YuanfengNous essayons d'être aussi informatifs que possible, mais ces informations ne sont pas destinées à remplacer les directives officielles des autorités de réglementation.

